- 上一篇:大塑性变形对铝合金的晶间腐蚀性能的影响
- 下一篇:层间交换偏置体系中反铁磁稀释效应的微磁学模拟
二氧化锰是一种晶格结构比较复杂的氧化物,目前己知的多种二氧化锰中,大多数是混合晶型,其氧化程度和水含量都是可变的。所以常用MnOx来表示其分子式,其中x为含氧量,其数值总是小于 2。通常,二氧化锰在其化学组成上还含有低价锰离子和OH-,而且有的还含有K+、Na+、Ba2+、Rb+、Li+、NH4+等金属离子。晶格常有缺陷,包括隧道和空穴。
1.1 光催化反应
1972年,Honda和Fujishima发现,在光辐射条件下,在TiO2半导体电极和金属电极所组成的电池中,可持续发生水的氧化还原反应,产生H2。这一发现表明通过半导体电可以将光能转化为化学能,随即人们对半导体在光作用下能否用于催化降解污染产生了兴趣。从七十年代初期以来,国外许多学者竞相开展这方面的研究。1976年,J.H.Carey报道了TiO2水浊液在近紫外光的照射下使多氯联苯脱氨,该体系在光照条件下可非选择性氧化降解各类有机物,生成CO2和H2O。大量研究表明,几乎所有的有机物都能有效的进行光催化反应,生成无毒的无机小分子物质,从而消除对环境的危害。
光催化反应基本可分为两种类型,就是敏化光反应和催化光反应。
敏化光反应指起始光激发发生在催化剂表面吸附的分子上,该分子再与基态催化剂本底反应。如果半导体是非光活性的,对于表面吸附的物质而言没有合适的能级,如SiO2等物质,半导体氧化物基体仅仅为光催化反应提供二维环境,而不参与光诱导电子过程,电子直接从吸附物想受体分子转移;如果半导体催化剂有合适的能级,并且半导体基底与被吸附物之间有强烈的电子相互作用,半导体基底将对光诱导电子迁移过程起调节作用,电子从给体迁移进入半导体光催化剂,然后再进入受体轨道,在这种情况下,光催化剂参与诱导电子的动力学过程。
催化光反应是指入射光首先激发半导体光催化剂,受激发的光催化剂再将光生电子或能量传递给吸附在其表面上的基态分子,然后在进行反应,光催化反应以n型半导体的能带理论为基础。半导体的能带结构通常由一个充满电子的低能价带和一个空的高能导带构成,价带和导带之间存在一个区域为禁带,区域的大小称为禁带宽度。当能量等于或大于禁带宽度的光照射半导体时,价带电子被激发跃迁到导带上,而在价带留下相应的空穴,形成光生电子空穴对,激发的电子和空穴迁移至半导体颗粒的表面,如果能带边缘位置符合某种要求,光生电子空穴就会与水或有机物发生氧化还原反应,即光催化降解反应。
1.2 二氧化锰的结构和分类
二氧化锰的骨架结构是[MnO6]八面体,氧原子在八面体顶点上,锰原子位于八面体中心,其结构如图 1-1以及图 1-2(a)所示。[MnO6]八面体基于氧原子构成六方紧密堆积或立方紧密堆积。在密堆积结构中,各原子层形成四面体和八面体的空穴。最常见的结构是[MnO6]八面体与相邻的八面体共用棱或共用顶角,而形成变化多端的复杂网络,这些网络可容纳各种不同的阳离子与配位物,因此造成了锰氧化物在组成和结构上的多样性。图 1-2 给出了几种不二氧化锰的结构示意图。
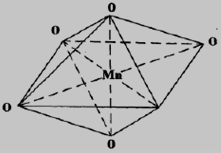
图 1-1 二氧化锰的骨架结构
根据[MnO6]八面体的连接方式和二氧化锰内部隧道结构的空间形态,可将二氧化锰分为三大类:一维隧道状(或链状)结构、二维层状(或片状)结构以及三维网络结构。
1.2.1一维隧道结构
一维隧道结构的二氧化锰是由[MnO6]八面体共棱连接形成沿C晶轴伸展的单链、双链或多链,链之间再通过共顶角相连,从而围成各种尺寸的一维无限隧道。这类链状或隧道状结构的化合物,包括α、β、γ、ε型等。在这类结构中,把未被占据的八面体晶格点形成的平行于C轴的空穴定义为隧道。S.Turner等建议把二氧化锰的各类隧道的命名用T[m,n]表示,T为隧道结构。m是隧道的高度,n是宽度,如β-MnO2,m=1,n=1,故隧道结构为T[1×1];α-MnO2,m=2,n =2,隧道结构用T[2×2]表示。