- 上一篇:多元金属/非金属掺杂的半导体TiO2的可见光光催化性能研究
- 下一篇:Cu2O复合材料的制备及其汽油脱硫性能研究
溶剂热法[ ]是指在密封的压力容器(如高压釜)中加入水或其它溶剂作为反应介质,通过加热在反应容器内创造一个高温高压的反应环境,使得通常难溶或不溶的物质能够在溶解后发生反应并重结晶,再分离和热处理重结晶产物得到纳米粒子。 该法的优点在于合成的纳米晶体晶粒发育完整,磁性较好,粒度分布均匀;其缺点是反应需在高温高压下进行,因此对设备要求也较为严格,生产成本相对较高,并且实现难以大批量生产。
四氧化三铁的晶体结构为反尖晶石结构,尖晶石铁氧体的化学分子式通式为M2+Fe23+O4[ ],即Fe3O4晶体结构中既有三价铁原子,又有二价铁原子。溶剂热法制备Fe3O4磁性纳米粒子,以FeCl3.6H2O为前驱体,提供铁源。一些极性无机物(包含氯化物)易溶解在HOC2H4OH (乙二醇,EG,极性溶剂)中,形成稳定的溶液;高温环境下,HOC2H4OH分子内发生脱水反应生成的具有还原性的乙醛,能将部分溶液中的Fe3+还原成为Fe2+;同时,HOC2H4OH分子间会发生聚合形成PEG(聚乙二醇),这样可有效降低粒子团聚的可能性[ ]。总的来说,作为溶剂的HOC2H4OH,也是还原剂。Ting Fan等人[ ]提出醋酸钠在反应中作为配体并在反应初期经历一个中间络合阶段,整个过程的反应式(200 ℃)如下:
2Fe3+ + Ac + 5H2O → Fe2O(Ac)(OH)3.H2O + 5H+ (反应式2.1)
Fe2O(Ac)(OH)3·H2O → 2FeOOH + HAc + H2O (反应式2.2)
4Fe2O(Ac)(OH)3·H2O + 3C2H6O2 → 8Fe + 3C2H2O4 + 4HAc + 14H2O (反应式2.3)
4Fe2O(Ac)(OH)3·H2O + C2H6O2 → 8Fe(OH)2 + C2H2O4 + 4HAc + 2H2O(反应式2.4)
2FeOOH → Fe2O3 + H2O (反应式2.5)
4Fe2O3 + Fe → 3Fe3O4 (反应式2.6)
2FeOOH + 8Fe(OH)2 → Fe3O4 + 2H2O (反应式2.7)
上述反应生成Fe3O4片层结构后,由于片层表面能趋于最小化,从而卷曲形成比表面积最小的球形。整个反应过程如图2.2所示:
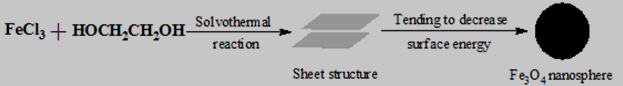
图2.1 以氯化高铁为铁源制得四氧化三铁纳米球机理简图
2.2 方案设计
2.2.1 实验试剂与仪器
表2.1 实验试剂一览表
药品名称 分子式 平均相对分子量 生产厂家 纯度
六水氯化高铁 FeCl3·6H2O 270.29 国药集团化学试剂有限公司 分析纯
无水醋酸钠 C2H3NaO2 82.03 上海凌峰化学试剂有限公司 分析纯
乙二醇 C2H6O2 62.07 上海试四赫维化工有限公司 化学纯
聚乙二醇 (OCH2CH2O)n
-
共轭反应硫酸软骨素-壳聚...
-
42CrMo典型风电主轴材料的等温正火工艺研究
-
Cu/Al复合材料界面组织特征研究
-
纳米粒子修饰的LSCF阴极材料研究
-
高性能锂离子电池LiNi0.5...
-
膨胀石墨的表面修饰与纳米复合材料的制备
-
铝基复合材料电子束焊工艺与界面性能
java+mysql车辆管理系统的设计+源代码
杂拟谷盗体内共生菌沃尔...
酸性水汽提装置总汽提塔设计+CAD图纸
乳业同业并购式全产业链...
电站锅炉暖风器设计任务书
大众媒体对公共政策制定的影响
十二层带中心支撑钢结构...
当代大学生慈善意识研究+文献综述
河岸冲刷和泥沙淤积的监测国内外研究现状
中考体育项目与体育教学合理结合的研究